En direct des laboratoires de l'institut de Chimie, communication du CNRS du 13 décembre 2018.
Publication des chercheurs du laboratoire du chimie dans la revue Chemical Sciences du 18 septembre 2018.
Il existe des mécanismes chimiques de protection de l’ADN face à la lumière UV. C’est ce qui a été mis en évidence par des équipes de scientifiques du laboratoire de physique et de chimie théorique (Université de Lorraine/CNRS) et de l’ENS Lyon, en association avec l’Université de Valence, en Espagne. Cette démonstration est une première. Elle pourrait trouver un intérêt dans la lutte contre les cancers de la peau.
Mieux vaut ne pas trop s’exposer au soleil. Cette phrase de prévention est répétée chaque année avant que les vacanciers ne viennent inonder les plages et elle est loin d’être vaine. La lumière UV a en effet un impact reconnu sur l’ADN. Son action met en jeu des mécanismes moléculaires qui débouchent sur des lésions de la molécule, ce qui peut mener à des cancers de la peau. Mais l’ADN sait se défendre ! Des scientifiques du laboratoire de physique et de chimie théorique (Université de Lorraine/CNRS) et de l’ENS Lyon, en association avec l’Université de Valence, en Espagne, ont mis en évidence une stratégie d’auto-protection basée sur un mécanisme qui n’avait jamais été identifié. La molécule à double hélice est capable d’interagir avec des ions sodium (qui sont omniprésents dans les cellules) pour activer des réactions chimiques, véritable contre-mesure à l’action de la lumière.
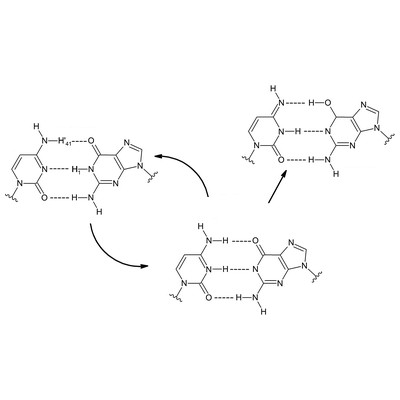
Cette découverte s’est faite en s’intéressant aux transferts de protons entre les paires des quatre bases qui forment le cœur des acides nucléiques de l’ADN (A/T et G/C). Ces transferts, déclenchés par des réactions chimiques causées par la lumière UV, amènent des mutations en créant un défaut qui sera retranscrit quand la cellule se divisera. Durant plus de 3 mois, 50 cœurs informatiques ont donc calculé les interactions de trois paires de bases, soit plus d’une centaine d’atomes modélisés dans le temps et l’espace. Un véritable microscope virtuel capable d’atteindre une précision inouïe. La maquette virtuelle a permis d’observer qu’il existait deux types de transfert. Le transfert simple, déjà connu, et le transfert double, qui lui dure environ une picoseconde. Ce double transfert (entre G et C) crée une base intermédiaire instable qui retransmet immédiatement les 2 protons à la base initiale. La rapidité de cet aller-retour empêche la création de défaut car il y a très peu de chance que la division cellulaire se déroule exactement au même moment. Pour les chercheurs, cette découverte est très intéressante car ce transfert "bénéfique" est accru par la présence d’ions sodium (Na+). Ils en concluent aussi que les protéines chargées positivement, autour desquelles l’ADN s’entortille, peuvent avoir un effet stabilisateur sur la molécule qui détient les codes du vivant.
Source : Dynamics of the excited-state hydrogen transfer in a (dG)·(dC) homopolymer: intrinsic photostability of DNA. Antonio Francés-Monerris, Hugo Gattuso, Daniel Roca-Sanjuán, Iñaki Tuñón, Marco Marazzi, Elise Dumont et Antonio Monari. Chemical Sciences, septembre 2018 DOI: 10.1039/C8SC03252A
Structures
Disciplines
Mots clés