Publication du LBMC dans Nature Cell Biology
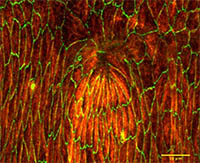
Vue dorsale d’un embryon de drosophile mutant pour le gène Zasp52 et marqué avec un anticorps anti-E-Cadhérine (vert) et un anticorps anti-tubuline (rouge). Le côté dorsal est fermé, mais la forme des cellules est irrégulière. Barre d’échelle= 10 microns. Photo © Antoine Ducuing.
Deux chercheurs du Laboratoire de Biologie et Modélisation de la Cellule (LBMC) confirment expérimentalement une hypothèse vieille d’un quart de siècle en démontrant que la structure cellulaire appelée câble d’actine permet de refermer les tissus sans cicatrice. La cicatrisation est parfaite car le câble répartit les forces de tension au niveau cellulaire sans pour autant agir sur la vitesse de fermeture. Il protège ainsi les cellules lors de la morphogenèse du tissu, et garantit leur intégrité physique. Ces résultats sont publiés dans la revue Nature Cell Biology du 17 octobre 2016.
Les embryons cicatrisent parfaitement, mais cette propriété se perd peu à peu au cours du développement. Bien que cette capacité soit exploitée en médecine lors d’opérations chirurgicales intra-utérines, comme la réparation du bec-de-lièvre ou de la fente palatine, nous n’en connaissons pas les bases moléculaires. Cependant, le mécanisme de réparation chez l’embryon corrèle avec la présence d’un câble qui entoure la plaie et qui n’a jamais été observé lors de la cicatrisation adulte. Ce câble, présent chez les embryons de multiples espèces, est formé d’actine, la composante principale de nos muscles. L’actine forme un filin au sein de chaque cellule, qui est relié d’une cellule à l’autre par des molécules d’adhérence. Le câble d’actine donne une cohésion d’ensemble et permet de passer d’une structure cellulaire à un niveau tissulaire.
Une hypothèse séduisante est que le câble agit comme un cordon de bourse qui accélère la fermeture de la plaie et conduit à une cicatrisation parfaite. Ce modèle est basé sur plusieurs observations, et en particulier sur la dynamique de la fermeture dorsale de l’embryon de la mouche du vinaigre. En effet, la fermeture dorsale ressemble à la cicatrisation et offre un système élégant pour étudier le câble chez l’animal vivant et les mouches transgéniques exprimant des protéines fluorescentes permettent de suivre le câble à chaque étape du processus. Les chercheurs de l’Ecole Normale Supérieure de Lyon ont récemment observé que ce câble est absent chez certaines mouches mutantes. Par contre, les autres structures organisées à partir de l’actine comme le cytosquelette, ne sont pas modifiées chez ce mutant. Les chercheurs ont ainsi eu une occasion unique de pouvoir analyser la fermeture dorsale d’embryons dont seul le câble est absent.
La première surprise a été d’observer au PLATIM que ces embryons se ferment. La seconde a été de constater que la vitesse de fermeture ne diminue pas en l’absence du câble. Le câble ne joue donc pas le rôle dynamique de cordon de bourse qui lui était associé depuis des décennies. Par contre, l’analyse fine en microscopie confocale montre qu’en l’absence de câble, les cellules du bord du tissu sont étirées, compressées et n’adoptent pas leur forme rectangulaire (figure). Ces cellules ne sont pas organisées de manière régulière et la polarité du tissu est perturbée. Lors de la différenciation de l’épiderme, les défauts perdurent et les soies qui recouvrent l’animal sont désorganisées. Ces défauts persistants sont caractéristiques d’une cicatrice.
Ces résultats démontrent que le câble prévient la formation de cicatrices et suggèrent un nouveau mécanisme. Les forces de réparation opèrent au niveau du tissu, à un ordre de grandeur bien supérieur à ce que peu tolérer une cellule. Si quelques cellules seulement sont soumises à ces forces de tension, elles perdront leur structure et leur faculté de former un tissu cohérent. Le câble permet au contraire d’homogénéiser les forces et de coordonner les cellules afin de conserver un tissu homogène et polarisé où chaque cellule est préservée.
Les chercheurs espèrent que ces conclusions pourront bientôt être étendues aux vertébrés. La question sera alors de savoir si l’on pourra un jour induire la formation d’un câble lors de la cicatrisation adulte pour améliorer son efficacité et limiter la formation des cicatrices.
Retrouver l'info "En direct des labos" sur le site du CNRS
Références : The actin cable is dispensable in directing dorsal closure dynamics but neutralizes mechanical stress to prevent scarring in the Drosophila embryo. Antoine Ducuing and Stéphane Vincent. Nature Cell Biology. doi:10.1038/ncb3421
Stéphane Vincent, Maitre de conférences, et Antoine Ducuing, doctorant, poursuivent tous les deux leurs recherches au LBMC, au sein de l'équipe Epithelial differentiation and morphogenesis in Drosophila dirigée par Muriel Grammont.
Deux chercheurs du Laboratoire de Biologie et Modélisation de la Cellule (LBMC) confirment expérimentalement une hypothèse vieille d’un quart de siècle en démontrant que la structure cellulaire appelée câble d’actine permet de refermer les tissus sans cicatrice. La cicatrisation est parfaite car le câble répartit les forces de tension au niveau cellulaire sans pour autant agir sur la vitesse de fermeture. Il protège ainsi les cellules lors de la morphogenèse du tissu, et garantit leur intégrité physique. Ces résultats sont publiés dans la revue Nature Cell Biology du 17 octobre 2016.
Les embryons cicatrisent parfaitement, mais cette propriété se perd peu à peu au cours du développement. Bien que cette capacité soit exploitée en médecine lors d’opérations chirurgicales intra-utérines, comme la réparation du bec-de-lièvre ou de la fente palatine, nous n’en connaissons pas les bases moléculaires. Cependant, le mécanisme de réparation chez l’embryon corrèle avec la présence d’un câble qui entoure la plaie et qui n’a jamais été observé lors de la cicatrisation adulte. Ce câble, présent chez les embryons de multiples espèces, est formé d’actine, la composante principale de nos muscles. L’actine forme un filin au sein de chaque cellule, qui est relié d’une cellule à l’autre par des molécules d’adhérence. Le câble d’actine donne une cohésion d’ensemble et permet de passer d’une structure cellulaire à un niveau tissulaire.
Une hypothèse séduisante est que le câble agit comme un cordon de bourse qui accélère la fermeture de la plaie et conduit à une cicatrisation parfaite. Ce modèle est basé sur plusieurs observations, et en particulier sur la dynamique de la fermeture dorsale de l’embryon de la mouche du vinaigre. En effet, la fermeture dorsale ressemble à la cicatrisation et offre un système élégant pour étudier le câble chez l’animal vivant et les mouches transgéniques exprimant des protéines fluorescentes permettent de suivre le câble à chaque étape du processus. Les chercheurs de l’Ecole Normale Supérieure de Lyon ont récemment observé que ce câble est absent chez certaines mouches mutantes. Par contre, les autres structures organisées à partir de l’actine comme le cytosquelette, ne sont pas modifiées chez ce mutant. Les chercheurs ont ainsi eu une occasion unique de pouvoir analyser la fermeture dorsale d’embryons dont seul le câble est absent.
La première surprise a été d’observer au PLATIM que ces embryons se ferment. La seconde a été de constater que la vitesse de fermeture ne diminue pas en l’absence du câble. Le câble ne joue donc pas le rôle dynamique de cordon de bourse qui lui était associé depuis des décennies. Par contre, l’analyse fine en microscopie confocale montre qu’en l’absence de câble, les cellules du bord du tissu sont étirées, compressées et n’adoptent pas leur forme rectangulaire (figure). Ces cellules ne sont pas organisées de manière régulière et la polarité du tissu est perturbée. Lors de la différenciation de l’épiderme, les défauts perdurent et les soies qui recouvrent l’animal sont désorganisées. Ces défauts persistants sont caractéristiques d’une cicatrice.
Ces résultats démontrent que le câble prévient la formation de cicatrices et suggèrent un nouveau mécanisme. Les forces de réparation opèrent au niveau du tissu, à un ordre de grandeur bien supérieur à ce que peu tolérer une cellule. Si quelques cellules seulement sont soumises à ces forces de tension, elles perdront leur structure et leur faculté de former un tissu cohérent. Le câble permet au contraire d’homogénéiser les forces et de coordonner les cellules afin de conserver un tissu homogène et polarisé où chaque cellule est préservée.
Les chercheurs espèrent que ces conclusions pourront bientôt être étendues aux vertébrés. La question sera alors de savoir si l’on pourra un jour induire la formation d’un câble lors de la cicatrisation adulte pour améliorer son efficacité et limiter la formation des cicatrices.
Retrouver l'info "En direct des labos" sur le site du CNRS
Références : The actin cable is dispensable in directing dorsal closure dynamics but neutralizes mechanical stress to prevent scarring in the Drosophila embryo. Antoine Ducuing and Stéphane Vincent. Nature Cell Biology. doi:10.1038/ncb3421
Les travaux des chercheurs
Stéphane Vincent, Maitre de conférences, et Antoine Ducuing, doctorant, poursuivent tous les deux leurs recherches au LBMC, au sein de l'équipe Epithelial differentiation and morphogenesis in Drosophila dirigée par Muriel Grammont.
Mots clés