
NLRP3 est un senseur de stress cellulaire participant à la détection des infections et la mise en place d’une réponse inflammatoire protectrice. Cependant, sa dérégulation nourrit de nombreuses pathologies à composante inflammatoire dont la goutte, le diabète, la maladie d’Alzheimer et l’athérosclérose. Ces travaux, publiés dans la revue Nature Communications, identifie la phosphorylation de NLRP3 comme un point de régulation clé qui pourrait à l’avenir être ciblé dans des stratégies anti-inflammatoires.
L’inflammation est généralement bénéfique pour l'organisme car elle participe à la réponse protectrice contre les infections et permet la réparation tissulaire. Cependant lorsque l'inflammation est chronique ou excessive, elle devient délétère. La réponse inflammatoire est déclenchée en aval de récepteurs spécialisés qui détectent les situations d’infections ou de lésions. Parmi ceux-ci, NLRP3 est un senseur de stress cellulaire impliqué dans la réponse à des infections très variés (virus, bactéries, champignons, parasites), mais également dans des auto-inflammations héréditaires (syndromes périodiques associés à la cryopyrine - CAPS), ou dans l’inflammation accompagnant la progression de pathologies multifactorielles telles que le choc septique, la goutte, l’athérosclérose, la maladie d’Alzheimer, et plus généralement l’inflammation délétère accompagnant le vieillissement. Suite à son activation, NLRP3 assemble un complexe nommé inflammasome constituant une plateforme d’activation pour la caspase-1. Cette protéase contôle alors la maturation et la sécrétion des cytokines inflammatoires IL-1b et IL-18, et une forme de mort cellulaire inflammatoire, la pyroptose, conduisant à la libération de nombreuses alarmines.
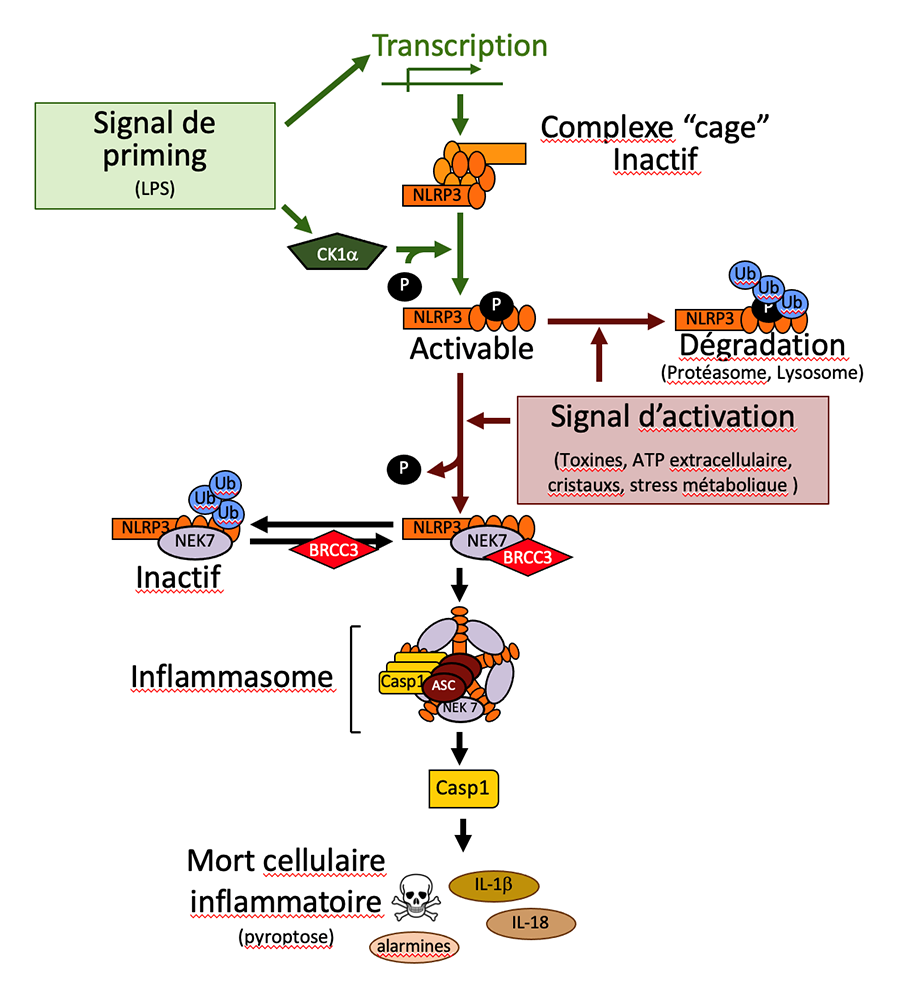
La diversité structurale des stimuli activateurs de NLRP3 exclut l’hypothèse qu’ils agissent par liaison directe à ce senseur tel un ligand, et malgré son fort potentiel thérapeutique, le mécanisme d'activation de NLRP3 n'est toujours pas compris. Il est maintenant admis que l’activation de NLRP3 est finement contrôlée par des modifications post-traductionnelles de NLRP3, par exemple l’attachement covalente de groupements phosphate (phosphorylation) ou de petites protéines nommées ubiquitine (ubiquitination) qui modifie les propriétés de surface des protéines et leur intéractome. Dans des conditions activatrices nécessitant deux signaux dits de priming et d’activation, un enchaînement de modifications post-traductionnelles de NLRP3 contrôle la formation et la dissociation d’une succession de complexes concomitant à un trafic de NLRP3 entre différents compartiments intracellulaires pour aboutir à l’assemblage de l’inflammasome final en un assemblage micrométrique ("speck") unique localisé au centrosome.
Les auteurs ont employé une approche de spectrométrie de masse pour rechercher les sites de modifications post-traductionnelles de NLRP3. Ils ont identifié (par criblage fonctionnel de mutant en macrophages humains et murins ) différents sites de phosphorylation et d’ubiquitination dont une sérine phosphorylée qui s’est avérée critique pour la réponse inflammasome. La phosphorylation de cette sérine est régulée de façon dynamique au cours du processus d’activation de NLRP3. Alors que sa phosphorylation initiale par la kinase CK1a permet de rendre NLRP3 sensible aux signaux d’activation, sa déphosphorylation ultérieure en réponse à ces derniers est critique pour l’assemblage de l’inflammasome. En effet, la déphosphorylation de cette sérine permet le recrutement de NEK7, un partenaire clé de NLRP3 au sein de l’inflammasome, et celui de la déubiquitinase BRCC3 qui permet de maintenir NLRP3 dans un état déubiquitiné actif. Les souris portant une substitution mimant la phosphorylation de NLRP3 sur cette sérine sont déficientes pour la réponse inflammatoire NLRP3 in vivo et sont résistantes au modèle de sepsis par choc endotoxique.
Ces résultats apportent une avancée conceptuelle dans la compréhension de la régulation de l’inflammasome et identifient la phosphorylation de NLRP3 par la kinase CK1a comme une potentielle cible thérapeutique anti-inflammatoire dans des pathologies très répandues.
Référence : NLRP3 phosphorylation in its LRR domain critically regulates inflammasome assembly. Tingting Niu, Charlotte De Rosny, Séverine Chautard, Amaury Rey, Danish Patoli, Marine Groslambert, Camille Cosson, Brice Lagrange, Zhirong Zhang, Orane Visvikis, Sabine Hacot, Maggy Hologne, Olivier Walker, Jeimin Wong, Ping Wang, Roméo Ricci, Thomas Henry, Laurent Boyer, Virginie Petrilli and Bénédicte F. Py. Nature Communications, 6 octobre 2021.
Disciplines
Mots clés






