Publication des travaux du CIRI dans la revue eLIFE le 19 juin 2018.
Dans un communiqué de presse du 27 avril 2018, la Direction générale de la Santé annonçait le renforcement de la surveillance du moustique tigre, aujourd’hui présent dans plus de 42 départements en métropole. Sa capacité à transmettre les virus de la Dengue, Zika ou Chikungunya, inquiète. De plus, une épidémie de Dengue sévit actuellement sur l’île de la Réunion. La lutte contre ce moustique vecteur d’infections est une première ligne de protection pour éviter l’établissement de cycles de transmission autochtones en métropole. Néanmoins, une meilleure connaissance des mécanismes de défense de notre organisme contre ces virus, qui contribue au développement de nouvelles applications thérapeutiques, est clairement indispensable.
L’étude de la réponse immunitaire contre ces virus est le principal sujet de recherche de l’équipe de Marlène Dreux, chercheuse Inserm au CIRI, Centre International de Recherche en Infectiologie (Université de Lyon, UCBLI, Inserm U111, ENS de Lyon, CNRS UMR5308). Avec ses collaborateurs au CIRI, à l’Institut Pasteur et Genentech à San Francisco, ils publient un article où ils décrivent le rôle de cellules sentinelles, les cellules dentritiques plasmacytodoïdes, dans le contrôle des infections par les virus de la Dengue et Chikungunya. Dans cette étude, ils utilisent un modèle d’étude expérimental original qui leur a permis de décrire pour la première fois le rôle de ces cellules pour contrer l’infection par ces virus : les cellules dentritiques plasmacytoïdes initient une réponse de défense par la production d’interféron, une molécule antivirale de l’hôte, qui va ensuite déclencher et accélérer une succession de réponses antivirales, notamment par d’autres types de cellules, et permettre un contrôle rapide de l’infection virale par le système immunitaire.
Les cellules dendritiques plasmacytoïdes (pDCs) ont la capacité de produire de grandes quantités d’interférons de type I par reconnaissance d’éléments des virus. Dans des études précédentes, l’équipe de Marlène Dreux avait démontré un mécanisme original d’activation des pDCs par les virus et, notamment, le virus de la Dengue [1] : les pDCs sont activées, non par une infection directe par le virus, mais par la reconnaissance des cellules infectées parcontact physique entre cellules infectées et les pDCs. C’est aussi le cas pour d’autres virus génétiquement éloignés [2, 3], ainsi que le virus du Chikungunya, comme démontré ici. Comment cette réponse par les pDCs, nouvellement découverte, contribue à l'élimination des infections virales et quelles sont les voies immunitaires impliquées sont des questions centrales à notre compréhension du contrôle des virus par les mécanismes de défense de l’hôte.
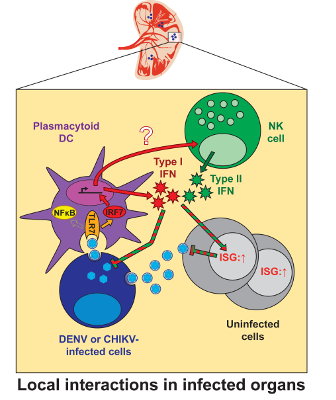
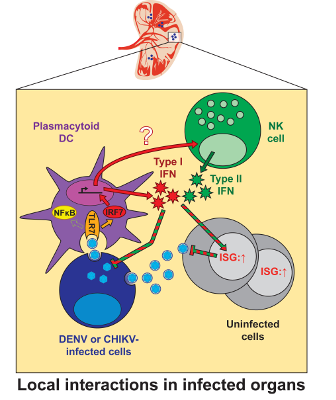
efficace. ©Brian Webster, CIRI
Les auteurs démontrent que la reconnaissance des cellules infectées par les virus de la Dengue et Chikungunya par les pDCs induit la production de grande quantité d’interferon de type I, mais pas d’autres molécules de défense, telles que de molécules dites pro-inflammatoires. Pour déterminer comment cette réponse affecte in vivo ces virus, les auteurs ont développé un modèle où la réponse de l’organisme par l’interferon de type I est limitée aux pDCs. Alors que les pDCs représentent un très faible pourcentage de toutes les cellules immunitaires, les auteurs démontrent qu'elles jouent un rôle important dans la réponse de première ligne contre les virus. Notamment, la réponse de défense par interféron déclenchée uniquement par les pDC permet la survie à l’infection par le virus Chikungunya, alors que son absence conduit à un phénotype lethal pour le modèle de référence déficient pour la réponse interféron de type I.
La réponse de défense des pDCs par production d'interféron, initialement confinée au site d’infection, alerte les cellules avoisinantes. Ainsi cette réponse est amplifiée et accélère les réponses antivirales par d’autres cellules immunitaires, telles que les cellules NK (natural killer). En coordonnant diverses réponses immunitaires, les pDCs orchestrent le contrôle des infections par la dengue et chikungunya in vivo.
Cette étude montre que les pDCs produisent de l'interféron de type I, une molécule de défense moins délétère pour l'hôte que d’autres molécules de l’immunité innée. La mobilisation de cette réponse par l’activation des pDCs, localisée au site d’infection et contribuant à la clairance virale in vivo, est d’intérêt pour la future conception de traitements contre ces virus. A cet égard, les auteurs démontrent in vitro que de faibles doses d'interféron accéléraient la réponse pDC contre le virus de la dengue, sans la production d'autres molécules préjudiciables à l'hôte.
Source : Plasmacytoid Dendritic Cells Control Dengue and Chikungunya Virus Infections via IRF7-regulated interferon responses. Webster B, Werneke SW, Zafirova B, This S, Coléon S,
Décembre E, Paidassi H, Bouvier I, Joubert P-E, Duffy D, Walzer T, Albert ML, Dreux M. eLIFE, 19 juin 2018. doi.org/10.7554/eLife.34273
Références :
- Sensing of immature particles produced by dengue virus infected cells induces an antiviral response by plasmacytoid dendritic cells. Décembre E, Assil S, Hillaire ML, Dejnirattisai W, Mongkolsapaya J, Screaton GR, Davidson AD, Dreux M. PLoS Pathog. 2014 Oct 23;10(10):e1004434. doi: 10.1371/journal.ppat.1004434
- Cell-Cell Sensing of Viral Infection by Plasmacytoid Dendritic Cells. Webster B, Assil S, Dreux M. J Virol. 2016 Oct 28;90(22):10050-10053.
- Short-range exosomal transfer of viral RNA from infected cells to plasmacytoid dendritic cells triggers innate immunity. Dreux M, Garaigorta U, Boyd B, Décembre E, Chung J, Whitten-Bauer C, Wieland S, Chisari FV. Cell Host Microbe. 2012 Oct 18;12(4):558-70.
Disciplines
Mots clés