
Publication des travaux du LBMC dans la revue Nature Communications.
Mieux comprendre le fonctionnement des protéines cellulaires.
Communiqué de presse de l'ENS de Lyon.
Les hélicases sont de véritables moteurs moléculaires à l’échelle d’une cellule. Leur carburant : l’ATP. Leurs fonctions : elles déshybrident des structures double brin d’acides nucléiques à la manière dont on ouvre une fermeture éclair, elles avancent le long de molécules simple brin d’ARN et/ou d’ADN et elles réorganisent des complexes composés de protéines et d’acides nucléiques. A ce titre, l’hélicase UPF1 est une protéine au cœur de multiples voies cellulaires impliquées dans le maintien de l’intégrité de l’ADN et de l’ARN. L’une d’elles, le nonsense mediated mRNA decay (NMD) peut dégrader des ARN messagers cellulaires. Plusieurs équipes dont celle de Pierre Jalinot (LBMC) ont également démontré que certains ARN viraux peuvent être soumis au NMD, notamment ceux du rétrovirus humain HTLV-1, responsable de 2 pathologies : un cancer de type leucémie ou une neuromyélopathie ; ainsi, le NMD constitue une nouvelle barrière cellulaire anti-virale.
Existe-t-il des contre-mesures mises en place par les virus pour se protéger de cette défense cellulaire ? Comment fonctionnement-elles ? Peut-on alors ce servir de ces enseignements pour mieux comprendre le fonctionnement des protéines cellulaires ? Ce sont là tous les enjeux du travail conjoint des biologistes et physiciens de l’ENS de Lyon (LBMC), de l’ENS de Paris (IBENS, LPS) et de l’IBCP (MMSB).
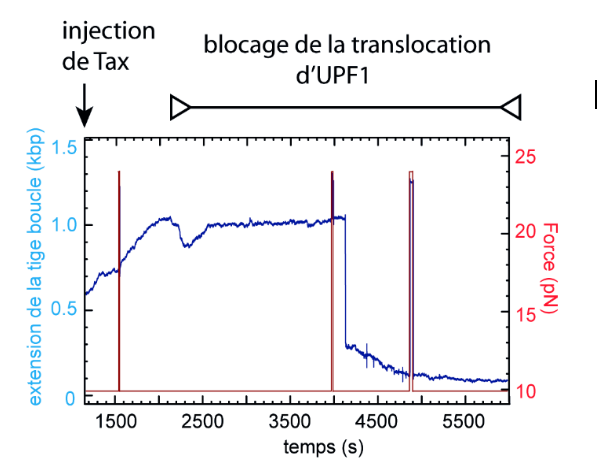
Dans cette étude, les chercheurs démontrent tout d’abord que la protéine virale Tax du rétrovirus humain HTLV-1 est capable d’inhiber le NMD ; ceci permettrait au virus de contourner cette menace tout en modifiant l’expression de certains gènes cellulaires à son avantage. Pour résoudre la question du "comment", ils ont combiné des approches de biochimie et de biologie cellulaire identifiant que Tax interagit avec le domaine central d’UPF1 et bloque son activité enzymatique. D’une part, la fixation de Tax à UPF1 obstrue la zone où l’hélicase se fixe aux acides nucléiques, empêchant le recrutement de cette dernière sur l’ARN. D’autre part, des approches de molécule unique suggèrent que Tax fige UPF1, quand l’hélicase est préalablement fixée à l’ARN : UPF1 devient moins sensible à la présence d’ATP et se bloque alors qu’elle avance le long de son substrat. Cette étude décrit donc une façon spécifique à HTLV-1 d’inhiber le NMD (d’autres virus ont développé des mécanismes alternatifs) et illustre l’importance de la translocation d’UPF1 sur l’ARN au cours de ce processus de dégradation de l’ARN. Elle ouvre également la voie à l’identification de nouvelles molécules ciblant l’interaction Tax/UPF1 pour renforcer la sensibilité du virus face à cette défense cellulaire.
Source :
Fiorini.F, Robin.J-P et al., (2018) HTLV-1 Tax plugs and freezes UPF1 helicase leading to nonsense-mediated mRNA decay inhibition. Nature Communications, 9:431.

Disciplines
Mots clés






